Bộ Y tế cấp phép cho nhập khẩu 30 triệu liều vắc-xin Hayat-Vax
Ngày 16/9, Cục Quản lý Dược (Bộ Y tế) đã cấp phép cho Công ty Cổ phần Y dược phẩm Vimedimex (quận 1, TP.HCM) nhập khẩu 30 triệu liều vắc-xin Hayat-Vax (Trung Quốc).
Ngày 10/9, Bộ Y tế phê duyệt có điều kiện vắc-xin COVID-19 Hayat-Vax cho nhu cầu cấp bách trong phòng, chống dịch bệnh COVID-19 tại Việt Nam, theo quy định tại Điều 67, Nghị định 54 ngày 8/5/2017 của Chính phủ.
Ngày 16/9, Cục quản lý Dược (Bộ Y tế) cấp phép nhập khẩu 30 triệu liều vắc-xin Hayat-Vax cho Công ty Cổ phần Y dược phẩm Vimedimex.
Theo báo Lao Động sáng 20/9, tại quyết định cấp phép, Cục Quản lý Dược cho biết nhận được Đơn hàng số 04/2021/ĐH-VMD ngày 11/9/2021 và các văn bản của Công ty Cổ phần Y dược phẩm Vimedimex về việc nhập khẩu vắc-xin chưa có giấy đăng ký lưu hành tại Việt Nam để đáp ứng nhu cầu cấp bách cho phòng, chống dịch bệnh theo quy định tại Điều 67 Nghị định số 54/2017/NĐ-CP (được sửa đổi, bổ sung tại Nghị định số 155/2016/NĐ-CP).
Cục Quản lý Dược đồng ý để Công ty Cổ phần Y dược Vimedimex nhập khẩu 1 vắc-xin tại Đơn hàng số 04/2021/ĐH-VMD ngày 11/9/2021, là vắc-xin Hayat-Vax, với số lượng 30.000.000 liều.
Cơ sở sản xuất bán thành phẩm là Beijing Institute of Biological Products Co., Ltd. (Trung Quốc); cơ sở đóng gói sơ cấp, thứ cấp và xuất xưởng là Julphar (Gulf Pharmaceutical Industries) (Các tiểu Vương quốc Ả rập thống nhất – UAE).
Cục Quản lý Dược yêu cầu Công ty Cổ phần Y dược phẩm Vimedimex phải thực hiện đúng các quy định hiện hành về xuất nhập khẩu, lưu thông phân phối thuốc và các quy định về dược có liên quan; phải chịu trách nhiệm về nguồn gốc, chất lượng vắc-xin nhập khẩu và bảo đảm việc sử dụng vắc-xin đúng mục đích, an toàn, hiệu quả theo đúng cam kết.
Các báo Đầu tư, Tuổi Trẻ ngày 20/9 xác nhận thông tin trên, kèm bài phỏng vấn PGS.TS. Trịnh Văn Lẩu, nguyên Viện trưởng Viện kiểm nghiệm thuốc Trung ương, nguyên Chủ tịch Hội đồng dược điển Việt Nam về chất lượng, hiệu quả của vắc-xin Hayat-Vax.
Ông Lẩu cho biết vắc-xin Hayat-Vax có hạn sử dụng là 12 tháng, và theo dữ liệu phân tích tạm thời, chế độ tiêm chủng 2 liều cách nhau 21 (+7) ngày, hiệu quả của vắc-xin Hayat-Vax là 78,89% (Khoảng tin cậy 95%: 65,79% ~ 86,97%).
“Tính an toàn của vắc xin Hayat-Vax được đánh giá thông qua các thử nghiệm lâm sàng tại Trung Quốc và quốc tế. Thử nghiệm lâm sàng giai đoạn tại Trung Quốc được kiểm soát song song ngẫu nhiên, mù đôi và giả dược để đánh giá sơ bộ tính an toàn, khả năng sinh miễn dịch của sản phẩm, cho người lớn từ 18 tuổi trở lên.
Thử nghiệm lâm sàng giai đoạn quốc tế, cụ thể là UAE thực hiện thử nghiệm lâm sàng 4Humanity. Đây là một thử nghiệm quốc tế đa trung tâm, đa chủng tộc, thu hút các tình nguyện viên đến từ hơn 125 quốc gia (trong tổng số hơn 45.000 tình nguyện viên), tình nguyện viên được ngẫu nhiên, mù đôi, được kiểm soát song song với giả dược để đánh giá hiệu quả bảo vệ, tính an toàn và khả năng sinh miễn dịch của sản phẩm này.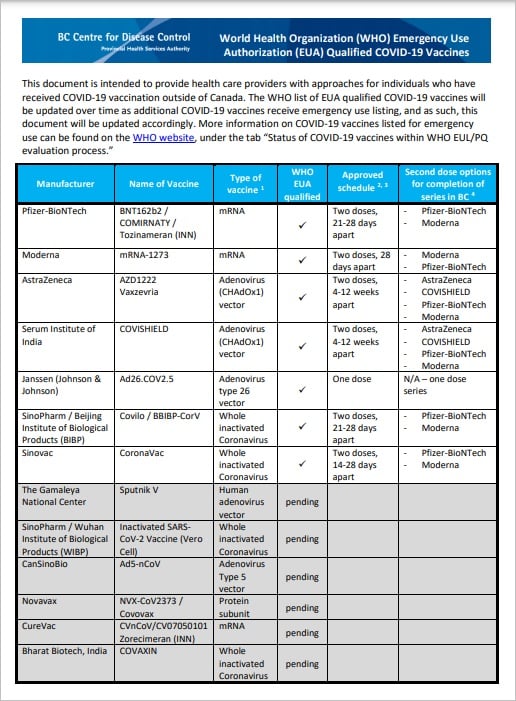
Theo dõi dữ liệu an toàn từ 0 – 21/28 ngày sau mỗi lần tiêm để quan sát sự xuất hiện của các tác dụng phụ, chú ý đến các tác dụng phụ nghiêm trọng xảy ra trong vòng 12 tháng sau khi tiêm chủng đủ liệu trình cùng một lúc. Dữ liệu phân tích tạm thời cho thấy, chế độ tiêm chủng hai liều cách nhau 21 (+7) ngày, hiệu quả của vắc-xin chống lại COVID-19 là 78,89% (KTC 95%: 65,79% – 86,97%).
Mức độ nghiêm trọng của tác dụng không mong muốn đối với sản phẩm này được quan sát trong các thử nghiệm lâm sàng chủ yếu là cấp độ 1 (mức nhẹ), tỷ lệ mắc tác dụng không mong muốn cấp độ 3 trở lên là 0,54%, không có tác dụng không mong muốn cấp độ 4 liên quan Hayat-Vax được báo cáo.
Tác dụng không mong muốn cấp độ 3 tại chỗ tiêm được báo cáo trong các thử nghiệm lâm sàng như đau, phát ban, ngứa; Tác dụng không mong muốn toàn thân cấp độ 3 sau tiêm chủng là sốt, mệt mỏi, nhức đầu, đau cơ, đau khớp, ho, khó thở, buồn nôn, nôn, tiêu chảy, táo bón, khó nuốt.” – báo Tuổi Trẻ dẫn thông tin.
Phân bổ 8 triệu liều vắc-xin Sinopharm: Hà Nội nhiều nhất với hơn 1,3 triệu liều
Ông Lẩu cho hay vắc-xin Hayat-Vax tới khi về Việt Nam và xuất xưởng là qua 6 lần kiểm tra chất lượng, trong đó:
Lần 1, Sinopharm thực hiện kiểm tra chất lượng bán thành phẩm theo tiêu chuẩn kỹ thuật đã được Sinopharm hoặc WHO phê duyệt trước khi vận chuyển đến UAE.
Lần thứ 2, Bộ Y tế UAE tiếp nhận kiểm tra và xác nhận “đạt tiêu chuẩn kỹ thuật”.
Lần thứ 3, Gulf Pharmaceutical Industries tại UAE thực hiện tiêm một lần kiểm tra chất lượng trước khi phân liều và đóng gói vào lọ.
Lần thứ 4, Bộ Y tế UAE kiểm tra chất lượng và phê duyệt từng lô vắc-xin Hayat-Vax để xuất khẩu, trước khi chuyển hàng sang Việt Nam.
Lần 5, Viện Kiểm định quốc gia vắc-xin và sinh phẩm y tế (Bộ Y tế) thẩm định trước khi nhập khẩu.
Lần 6, sau khi nhập khẩu về Việt Nam, Viện Kiểm định Quốc gia vắc-xin và sinh phẩm y tế lấy mẫu vắc-xin Hayat-Vax để kiểm định và cấp Giấy chứng nhận xuất xưởng – các báo Tuổi Trẻ, báo Đầu tư dẫn cùng thông tin.
Nguyễn Quân
Xem thêm:
Israel: Người tiêm đủ vắc-xin có nguy cơ nhiễm COVID-19 cao gấp 13 lần người từng nhiễm tự nhiên
Từ khóa vắc-xin Trung Quốc Dòng sự kiện Vắc-xin Hayat-Vax

































